单克隆抗体是生物制药行业正在开发的一类新兴疗法。自1986年首次获批以来,到2015年,已有近60种抗体在全球上市。仅在2016年,FDA就批准了另外7种治疗性抗体作为新的分子实体,几乎占当年批准的新药总数的三分之一。单克隆抗体的开发主要用于治疗炎症/自身免疫疾病和肿瘤适应症,并在较小程度上用于治疗其他疾病,如传染病和神经疾病。随着免疫治疗技术和蛋白质工程的进一步发展,单克隆抗体是制药行业中增长最快的一类治疗方法。
单克隆抗体包含数百种氨基酸,其中任何一种的变化都可能导致效力降低或安全性增加的担忧。与传统的小分子药物不同,抗体要大得多(约150 kDa),并且在细胞培养生产、纯化和储存过程中会发生广泛的酶促和非酶促反应,可能导致蛋白质变异。最常见的变异包括N端焦谷氨酸(pE)形成,蛋氨酸(M)氧化,天冬酰胺(N)脱酰胺化,天冬氨酸(D)异构化,C端赖氨酸(K)截断和糖基化。
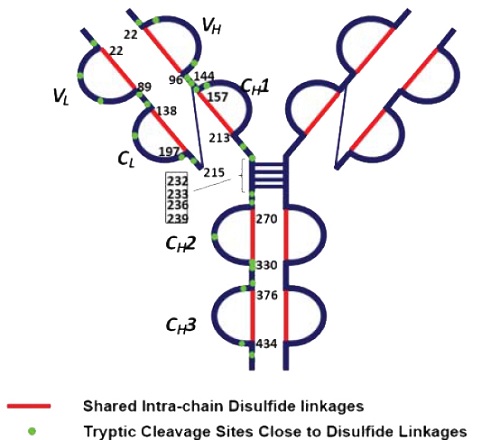
在生产工艺开发过程中,已经报道了许多序列突变和末端肽截短的例子。因此,开发可靠的分析方法来精确测量这些变异,以支持单克隆抗体的生产和最终产品的表征是非常重要的。由于单克隆抗体结构复杂,生产工艺复杂,因此与传统的小分子抗体相比,单克隆抗体治疗方法的开发具有更大的挑战性。分析单克隆抗体最常用的工具是基于电荷的分离技术,包括毛细管等电聚焦和离子交换色谱。研究这些分离的电荷变体通常需要一种自下而上的基于肽图谱的方法,包括反相液相色谱与串联质谱检测(RPLC-MS/MS)。
多肽定位在单克隆抗体鉴定中起着关键作用,例如提供翻译后修饰、序列改变等信息。结合质谱仪,肽图谱是最常用的表征工具,进一步研究不同抗体电荷变体形成的根本原因。在多肽定位中,单克隆抗体首先被胰蛋白酶等酶消化成短肽,然后用 RPLC-MS/MS 进行分离和鉴定 RPLC-MS/MS 在多肽分离方面已经建立了良好的分离能力。
Aimsmas的分析专家可以提供清晰简洁的肽图谱分析报告,帮助客户检测蛋白质水平结构、氨基酸序列等。
实验流程 |
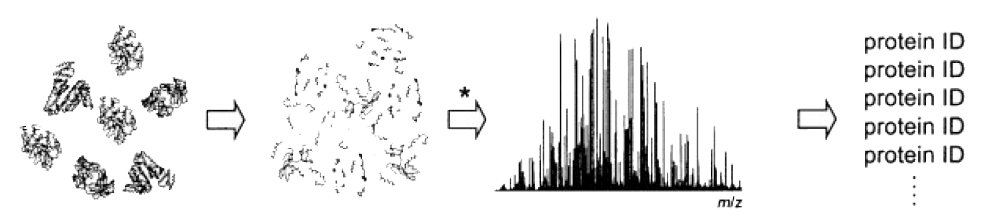 |
服务流程 |
|