蛋白序列分析
靶向代谢组实验专注于测定代谢物。三重四极杆质谱仪提供化合物确认所需的宽动态范围,高灵敏度以及出色选择性,是最佳选择。AIMS质谱提供专业的LC-MS和GC-MS服务,可为科研工作者提供下述代谢物质检测。
约 5–7 个工作日 空白 & 标准品 数据库检索 + 报告

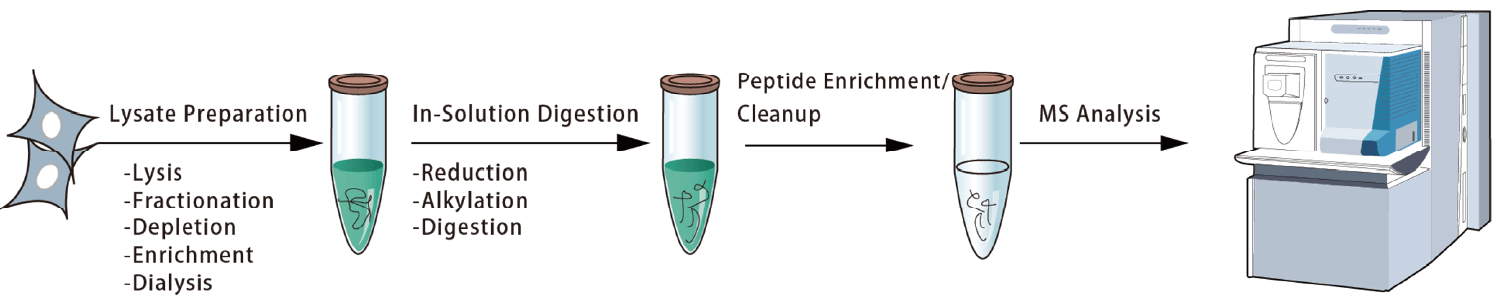
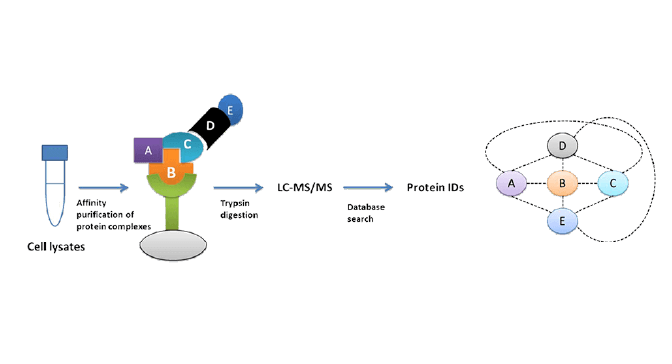
适用于细胞裂解液、免疫沉淀洗脱液以及缓冲液中的蛋白混合物。相较凝胶内酶解, 溶液法流程更简洁、肽段损失更少, 从而在更短时间内获得更深的蛋白组覆盖。
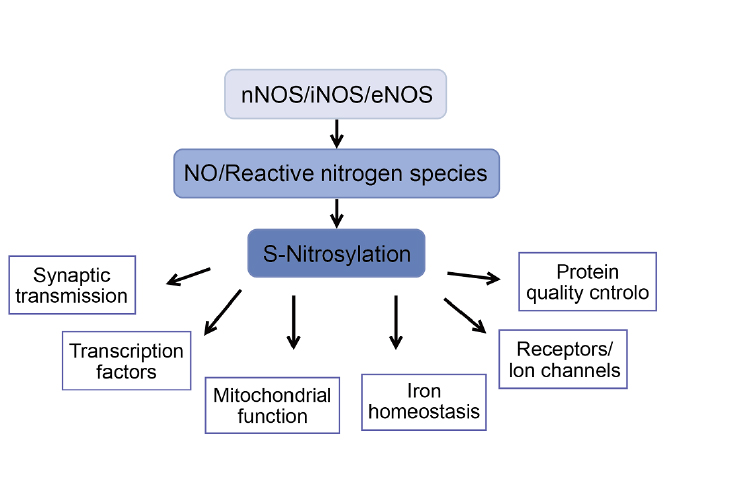
一氧化氮(NO)是诸如血管舒张, 血小板聚集抑制, 神经传递, 抗菌活动等一系列生理学过程的重要调控因子, NO的氧化还原状态及其二原子的化学性质, 使其能通过与各种蛋白质发生反应并调控各种细胞内和细胞外事件。很显然, NO修饰反应是通过将亚硝基集团转移至半胱氨酸的巯基上形成S-亚硝基硫醇(SNO), 这一过程通常被称之为S-亚硝基化作用。被大家公认的是蛋白发生S-亚硝基化的调控与磷酸化类似, 尽管蛋白中的半胱氨酸残基都可发生S-亚硝基化修饰, 但是只有很少的修饰是特异性的并且起到调控蛋白功能的作用。
目前最广泛阐明的NO信号通路机制包括对血红素蛋, 可溶性鸟苷酸环化酶以及细胞色素C氧化酶的结合和改变。蛋白S-亚硝基化是一种可逆的翻译后修饰, 被认为是蛋白质活动, 定位, 蛋白稳定性和蛋白之间互作的调节剂。
蛋白质的硫醇残基可以通过与NO集团和不同的硫醇底物发生特定反应形成S亚硝基硫醇, 其可以直接与NO作用也可通过在硫醇盐和S-亚硝基谷胱甘肽(GSNO)反应时形成。由于此过程的可逆性, 后一种化合物GSNO也同样促进S-亚硝基化反应, 因此会在氧化还原对GSH/GSNO和氧化还原对蛋白-SH/蛋白-SNO之间产生一种动态平衡。其实GSNOR通过与GSNO反应生成氧化谷胱甘肽二硫化物(GSSG)和氨(NH3), 因此而降低S-亚硝基醇的浓度, 随后谷氧还蛋白(GRX)通过将GSSG还原为GSH, 维护并稳定这个SNO的系统。 当然一氧化氮(NO)分子集团也可以直接转移到蛋白上发生修饰, S-亚硝基硫醇的动态平衡同样依靠于硫氧化还原蛋白/硫氧化还原蛋白还原酶(Trx/TrxR)系统, Trx-介导的SNO蛋白还原化为硫醇是通过对NAPDH的氧化为代价, 最终并产生NO去介导相关信号通路。
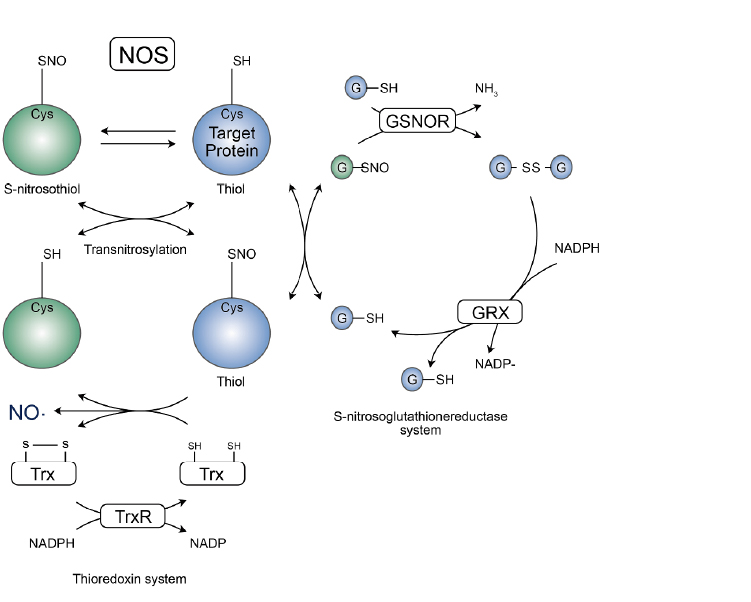
蛋白质的硫醇残基可以通过与NO集团和不同的硫醇底物发生特定反应形成S亚硝基硫醇, 其可以直接与NO作用也可通过在硫醇盐和S-亚硝基谷胱甘肽(GSNO)反应时形成。由于此过程的可逆性, 后一种化合物GSNO也同样促进S-亚硝基化反应, 因此会在氧化还原对GSH/GSNO和氧化还原对蛋白-SH/蛋白-SNO之间产生一种动态平衡。其实GSNOR通过与GSNO反应生成氧化谷胱甘肽二硫化物(GSSG)和氨(NH3), 因此而降低S-亚硝基醇的浓度, 随后谷氧还蛋白(GRX)通过将GSSG还原为GSH, 维护并稳定这个SNO的系统。 当然一氧化氮(NO)分子集团也可以直接转移到蛋白上发生修饰, S-亚硝基硫醇的动态平衡同样依靠于硫氧化还原蛋白/硫氧化还原蛋白还原酶(Trx/TrxR)系统, Trx-介导的SNO蛋白还原化为硫醇是通过对NAPDH的氧化为代价, 最终并产生NO去介导相关信号通路。
无标定量/谱计数 污染物过滤 支持自定义数据库
采用Thermo Fisher 高精度高分辨质谱仪, 可对蛋白序列进行精度检测, 上机时长120min更高的肽段覆盖率。
样本准备简单, 检测周期短, 约一周出报告。
若检测结果明显是质谱问题, 可免费重启上机一次。
Advantages
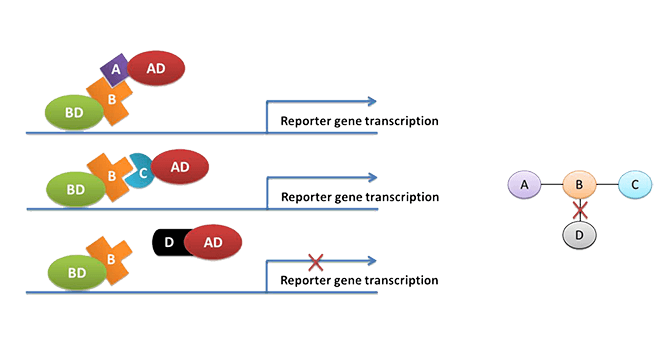
用于高通量互相蛋白筛选 直接检测两个蛋白互相作用
2D
发现互作蛋白的数量有限
在实际细胞内部可能并不发生互相作用
不能发现蛋白非直接相互作用
Advantages
用于高通量互相蛋白筛选 直接检测两个蛋白互相作用
2D
发现互作蛋白的数量有限
在实际细胞内部可能并不发生互相作用
不能发现蛋白非直接相互作用
查找有关试剂和一些常见使用规范常见问题解答, 如您找不到相关内容, 您可以了解我们在线客服.